國際認證再強化,微體生醫啟動歐盟新法規IVDR第一階段認證作業
2022-05-12
歐盟執委會已於前幾年公告將於2022年5月26日起,適用新的體外診斷醫療器材法規,簡稱IVDR,將取代原來的體外診斷醫材指令IVDD,大幅提升對醫療器材廠商的法規及品質管理要求。
與舊制相比,新制強調採用臨床資料以處理安全性問題,增加更為嚴格的認證機構指定規則外,並針對國家主管部門和歐委會增添更多的控制與監測要求,用以明確定位廠商、進口商、授權代表的權利與義務。
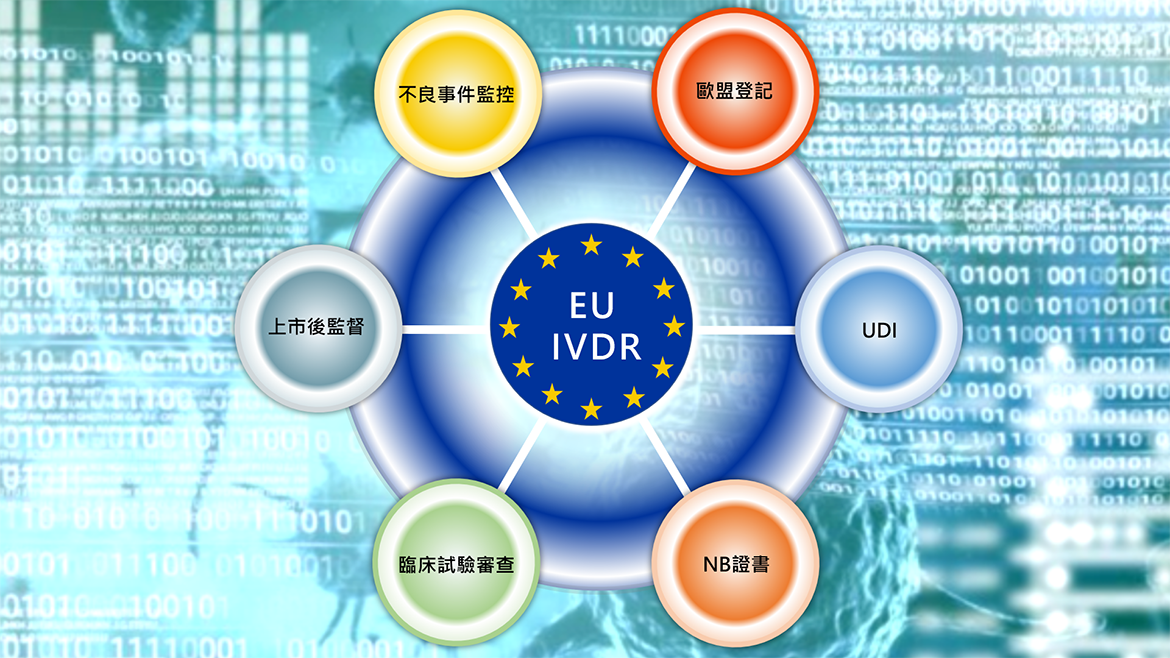
新制認證的取得必須符合:歐盟登記、UDI(醫療器材單一識別系統)、NB證書、臨床試驗審查、上市後監督、不良事件監控等必要條件。現今歐盟審查機構能量不足加上申請難度大幅增加的情況下,新制認證的取得將可能嚴重延滯。
因此,微體生醫提前布局,並於今日送出第一階段的審查資料,透過取得嚴格審查的歐盟新制認證,不僅能證明微體生醫是一家具有健全的品質管理體制,且產品安全穩定的公司,更能取得搶進國際市場的先機。


 歐盟執委會已於前幾年公告將於2022年5月26日起,適用新的體外診斷醫療器材法規,簡稱IVDR,將取代原來的體外診斷醫材指令IVDD,大幅提升對醫療器材廠商的法規及品質管理要求。
歐盟執委會已於前幾年公告將於2022年5月26日起,適用新的體外診斷醫療器材法規,簡稱IVDR,將取代原來的體外診斷醫材指令IVDD,大幅提升對醫療器材廠商的法規及品質管理要求。